伴隨生命的演化,免疫系統日趨復雜🤷。4.5億年前👮🏽♂️,魚類率先衍生出基於T、B細胞的適應性免疫系統;這種體系在漫長的進化中被繼承和發揚🖤,成為四足動物免疫防禦的準則🚶🏻♂️➡️。然而,比較基因組學的證據顯示,適應性免疫的左膀(T細胞)和右臂(B細胞),似乎經歷了截然不同的進化模式👩🔬。B細胞免疫隨著物種的演化而逐步完善,這不僅體現在新型免疫球蛋白、生發中心的依次出現,更體現在抗體親和力成熟、類型轉換等機製的相繼獲得。相比之下,T細胞的種類及核心組件🙎🏼,在硬骨魚向四足動物進化的過程中卻基本保持一致🙇🏼♂️♑️。回顧4.5億年的進化歷程,自然選擇的壓力造成了五次物種大滅絕,使得四足動物與魚類在免疫器官🫄🏻、生存環境🧑🏽🎓、膳食結構等方面產生了巨大變化😊。為應對這些挑戰,B細胞免疫的進化與完善並不難以理解🧖🏽,而T細胞免疫的穩定遺傳則顯得愈發神秘。
近日,顺盈娱乐生命科學學院楊嘉龍團隊在 Advanced Science 上發表了題為 Glutamine metabolism underlies the functional similarity of T cells between Nile tilapia and tetrapod 的研究論文🆙,揭示了T細胞免疫的進化規律。作者以羅非魚、非洲爪蟾🤷🏻、雞🥓、小鼠等動物為研究對象,試圖回答兩個科學問題:(1)比較基因組層面的T細胞穩定進化假說👸,是否體現在免疫學過程🍸、功能和調控機製上?(2)維持T細胞免疫穩定進化的潛在驅動力是什麽?

作者首先以低等脊椎動物羅非魚為模型🌆,描繪了早期T細胞免疫的概況。羅非魚T細胞通過動態增殖和凋亡,形成了典型的初次、記憶免疫應答;魚類T細胞的完全活化依賴第一、第二信號的協同作用,並由Ca2+-NFAT👺、MAPK/ERK、NF-kB和mTORC1通路共同調節;選擇性耗竭模型表明IgM+B細胞可向T細胞遞呈抗原⚜️,確保T細胞的活化和增殖。在功能上,魚類T細胞具備特異性殺傷靶細胞的細胞毒性功能📘,並可輔助IgM+B細胞的增殖和抗體分泌💃🏽。這些結果表明🍫,T細胞免疫的核心策略早在硬骨魚中即已確立👩🏽🍳。

谷氨酰胺代謝調控硬骨魚和四足動物T細胞免疫
為了解析魚類T細胞免疫的調控機製🎓,作者進行了轉錄組學分析👩🏽🚀。結果顯示,羅非魚使用了與哺乳動物相似的轉錄調控網絡支持T細胞免疫👨🏭👨🏿🦲;而病原感染羅非魚後🤱🏽,T細胞的差異表達基因主要富集於代謝通路👩🏿⚕️,且發生了大規模的代謝重編程。由於重編程的代謝程序均直接或間接溯源至谷氨酰胺分解代謝,進而探討了谷氨酰胺代謝對羅非魚T細胞免疫的調控👨🏿🎓。活化的羅非魚T細胞增加了谷氨酰胺的利用;而谷氨酰胺剝奪或谷氨酰胺酶GLS1的抑製,造成了T細胞增殖和效應功能的障礙。進一步的研究證實,mTORC1和MAPK/ERK通路承接了TCR信號🫅🏻,通過c-Myc調控谷氨酰胺代謝🧑🏻🦼➡️,並促進羅非魚T細胞免疫👩🦽。
基於羅非魚與哺乳動物在T細胞代謝及重編程方面的相似性,作者猜測:谷氨酰胺代謝調控T細胞免疫可能是有頜脊椎動物進化中的保守策略🕵🏼♂️。為了驗證這一猜測👩🏿⚖️,作者選取不同進化階段的脊椎動物,分析了谷氨酰胺代謝與T細胞免疫的關聯。結果表明,羅非魚🏌🏿、非洲爪蟾、雞和小鼠共享了保守的c-Myc驅動谷氨酰胺代謝以調控T細胞免疫的機製。此外🚐🎸,c-Myc或GLS1的敲降損害了人類JurkatT細胞的激活和增殖,而使用羅非魚的相應分子重建谷氨酰胺代謝途徑✊,能夠挽救人類T細胞的免疫缺陷。該發現為理解T細胞免疫的進化提供了新視角🛫,也為幹預人類免疫缺陷提供了潛在途徑🧱🫑。
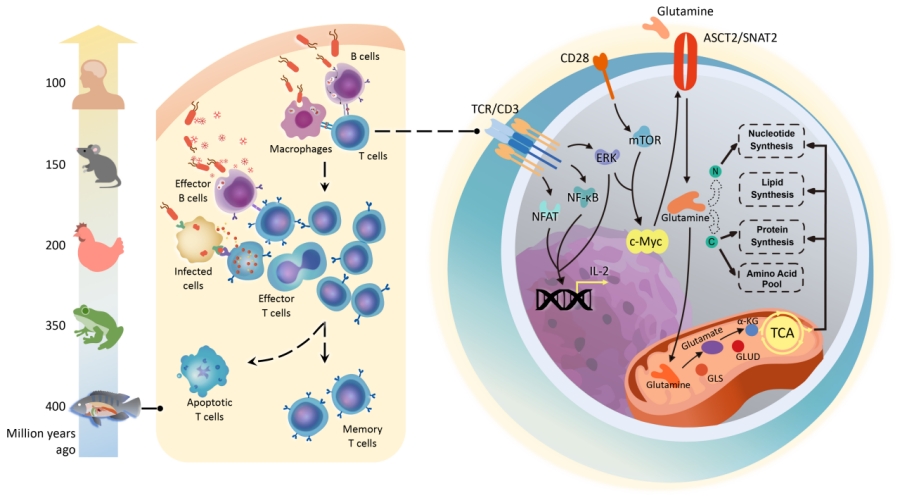
谷氨酰胺代謝是硬骨魚和四足動物之間T細胞功能相似性的分子基礎
綜上所述,該研究驗證了T細胞免疫穩定進化的假說,並提出保守的轉錄調控網絡和代謝程序🥈,尤其是谷氨酰胺分解代謝,是硬骨魚與四足動物之間T細胞功能相似性的分子基礎。該研究被選為Advanced Science的卷首文章。

卷首圖寓意:在硬骨魚(鯉魚)進化(躍龍門)為四足動物(龍)的過程中✍🏼,T細胞免疫基本不變,保守的谷氨酰胺(分子式)代謝途徑為這種穩定進化奠定了分子基礎。該圖由顺盈娱乐美術學院博士生賈點墨繪製🏋🏼👩👧👦。
顺盈娱乐生命科學學院博士研究生李康、韋秀梅副教授💂🏼♂️、碩士研究生焦新迎,和溫州醫科大學鄧文海博士為本文的共同第一作者🧑🏼⚕️,顺盈娱乐楊嘉龍教授為本文通訊作者🏂🏿。該研究受到國家自然科學基金優秀青年科學基金項目👷🏿♀️、面上項目等資助。

楊嘉龍教授🃏🤹♀️、博士研究生李康、碩士研究生焦新迎、韋秀梅副教授
論文鏈接🦇:
https://doi.org/10.1002/advs.202201164
圖文、來源丨生命科學學院、科技處 編輯丨杜玥 編審丨郭文君